I dati mostrano che, tra i pazienti che hanno completato l'estensione in aperto, i miglioramenti clinici osservati dopo le prime 24 settimane di terapia si sono mantenuti fino al termine delle 52 settimane.
Il trial ha valutato efficacia e sicurezza del farmaco in 201 pazienti, di cui 108 trattati con baricitinib 4 mg e 93 con baricitinib 8 mg una volta al giorno per un massimo di 52 settimane. Il dosaggio poteva essere aumentato fino a 8 mg al giorno dopo 28 o 32 settimane, a discrezione dello sperimentatore, se il paziente presentava più di sei articolazioni dolenti e tumefatte.
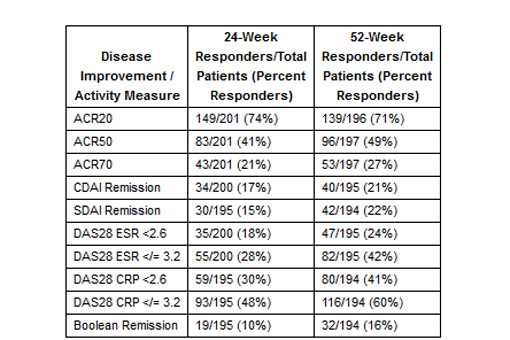
Dei 201 pazienti, 184 hanno completato l'estensione di 52 settimane, 15 hanno sospeso il trattamento e due non lo hanno ancora completato. Come riportato in precedenza, nelle prime 12 settimane dello studio baricitinib si è associato a miglioramenti statisticamente significativi dei segni e sintomi dell'AR rispetto al placebo e questa risposta si è mantenuta o è ulteriormente migliorata nelle successive 12 settimane di trattamento in cieco. I miglioramenti clinici osservati alla settimana 24 si sono poi mantenuti fino alla 52ma settimana. Infatti, la risposta ACR20 è risultata del 74% dopo 24 settimane e 71% dopo 52 settimane, l'ACR50 rispettivamente del 41% e 49% e l'ACR70 del 21% e 27%.
Anche tutte le altre misure di attività e miglioramento della malattia (indice di remissione CDAI, indice di remissione SDAI, DAS28CRP ≤ 3,2, DAS28CRP < 2,6, DAS28ESR ≤ 3,2, DAS28CRP < 2,6, remissione secondo i criteri Boolean ACR/EULAR) sono risultate simili all'inizio e alla fine dell'estensione, o addirittura migliorate al termine dello studio. Questo miglioramento è da ascrivere soprattutto a un aumento della risposta clinica ottenuto grazie a un aumento della dose di farmaco nei pazienti che nelle prime 24 settimane in doppio cieco erano stati trattati con placebo, oppure con baricitinib 1 mg o 2 mg una volta al giorno.
Quanto alla sicurezza, i segnali osservati durante l'estensione in aperto sono stati coerenti con quelli già riportati in precedenza per baricitinib. Tra i pazienti che hanno continuato il trattamento con 4 mg, l'incidenza degli eventi avversi è stata del 53% (57 pazienti) quella degli eventi avversi gravi del 10% (11 pazienti), quella delle infezioni del 31% (34 pazienti) e quella delle infezioni gravi del 4% (quattro pazienti). Tra quelli che hanno continuato con 8 mg, invece, le percentuali corrispondenti sono state del 63% (59 pazienti), 9% (otto pazienti), 40% (37 pazienti) e 2% (due pazienti). Non sono state osservate infezioni opportunistiche o casi di tubercolosi, ma c'è stato un decesso nel gruppo baricitinib 8 mg a causa di un sospetto infarto miocardico. "In questo studio clinico, baricitinib ha mostrato miglioramenti statisticamente e clinicamente significativi delle caratteristiche di questa condizione, che si sono mantenuti nell'arco di un anno di trattamento. Fino ad oggi, baricitinib ha dimostrato un profilo di sicurezza accettabile e gli effetti collaterali sono generalmente semplici da gestire. Questi risultati incoraggianti giustificano ulteriori studi su questo nuovo farmaco per l'artrite reumatoide" ha dichiarato il primo autore dello studio Peter Taylor, reumatologo dell'Università di Oxford.
Baricitinib appartiene a una nuova classe di farmaci, quella degli inibitori delle Janus chinasi (JAK), e in particolare è un inibitore selettivo delle chinasi JAK1 e JAK2, attivo per via orale. Il farmaco è già entrato in fase III come potenziale trattamento per l'AR ed è al momento in fase II anche come possibile terapia per la psoriasi e la nefropatia diabetica.
P. Taylor, et al. Baricitinib, an Oral Janus Kinase Inhibitor, in the Treatment of Rheumatoid Arthritis: Safety and Efficacy in Open-Label, Long-Term Extension Study. EULAR 2013; abstract OP0047.
leggi
Guarda le slide presentate all'EULAR
Torna all'archivio
